Topforsker om coronavaccine: Jeg sætter gerne min egen krop ind på det
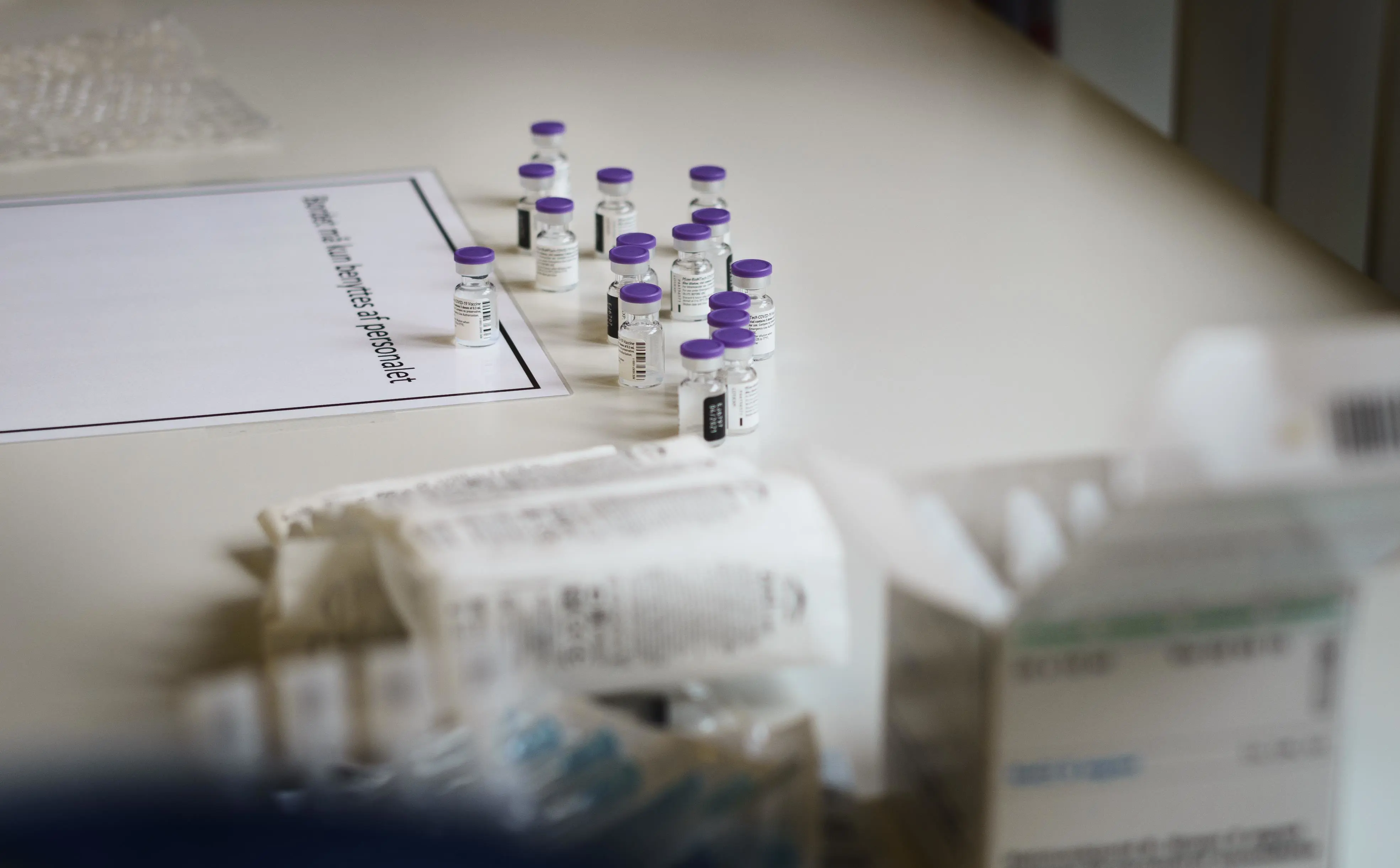
Der er ikke tale om en forhastet proces. Hverken i udvikling eller i godkendelsen af de nye coronavacciner, siger professor Jens Lundgren, der her svarer på nogle af de spørgsmål og bekymringer, som de nye vacciner kan give.
03. december 2020
Der er ingen danskere, der bliver forsøgskaniner, når de første corona-vacciner bliver tilbudt landets frontpersonale, ældre borgere og kronisk syge.
Det bliver med præcis samme sikkerhed, som alle de velkendte vacciner, vi bruger, selv om denne vaccine er udviklet og godkendt på rekordtid.
Læs også: Frontpersonale og ældre får tilbudt coronavaccine først
Det forsikrer professor Jens Lundgren, der lige som hundredvis af topforskere verden over venter utålmodigt på at gennemtrawle de enorme mængder data, som vil blive frigivet i løbet af december fra vaccineproducenterne Pfizer/BioNtech og Moderna. Råmateriale, der ligger til grund for de rapporter, som Det Europæiske Lægemiddelagentur EMA skal træffe afgørelse om den 29. december og 12. januar.”Mængden af viden, der bliver offentliggjort inden for den næste måned er gigantisk. Når resultaterne ligger åbent tilgængelige, kan vi ikke bare se hver vaccine for sig selv, men også på tværs af vacciner,” siger Jens Lundgren, der er professor i infektionssygdomme og overlæge på Rigshospitalet ved Infektionsmedicinsk klinik om den kommende tid, der for ham og hans forskerkolleger bliver ’vanvittigt interessant’.
Læs også: Søren Brostrøm: Sosu'er skal hjælpe med at vaccinere mod covid-19
Har ikke slækket på grundighedenFor der kan stadig ske meget, inden virksomhederne får en betinget markedsføringstilladelse af EMA, der er grundlag for, at de første borgere i Europas 27 medlemslande får adgang til den. Og altså også inden vaccinerne kan blive tilbudt til de ældre borgere, kronisk syge og frontpersonale i sundheds- og ældresektoren i Danmark, som ifølge sundheds- og ældreminister Magnus Heunicke vil få tilbudt vaccinen som de første.
”Jeg har oplevet de her godkendelsesprocesser flere gange i min karriere, og der er jo nogle gange, hvor der bliver stillet spørgsmål ved selve høringen, som gør, at man ikke kan træffe beslutningen om at godkende,” siger Jens Lundgren.
Læs også: FOA-faggrupper på hospital bliver testet for corona-immunitet
- Så selv om man siger, at vaccinerne bliver godkendt til markedsføring 29. december og 12. januar , så er det ikke sikkert, at det sker?”Nej, det er ikke 100 procent sikkert. I og med at processen her er speedet op, så vil materialet blive vurderet og læst helt op til den dato. Og hvis der er nogle spørgsmål, der ikke kan afklares, så må man gå tilbage og få det afklaret. Sådan er det. Myndighederne er ekstremt interesserede i, at alle kan følge med i, hvad præmisserne for godkendelsen er. Fik vi stillet alle de spørgsmål, der skal til? For de har brug for at være hundrede procent sikre på, at deres beslutningsgrundlag er uantasteligt.”
Læs også: Sosu-opgave mod influenza-dødsfald
- Men når du siger, at processen er fremskyndet, betyder det, at man er mindre grundig?”Nej, absolut ikke. Man er præcis lige så grundig, som man altid er, når man udvikler og godkender et lægemiddel eller en vaccine. Men man har taget en langt større økonomisk risiko. Og det siger måske sig selv, hvorfor: Firmaerne, regeringerne og myndighederne har haft en fælles interesse i virkelig at sætte turbo på. Det, der normalt tager tre, fire og fem år, tager nu et halvt. For eksempel er Lægemiddelstyrelserne villige til at lave en vurdering, som normalt vil tage dem cirka ni måneder på mindre end en måned, fordi de sætter 10 gange så mange medarbejdere til at vurdere det. Vurderingen er altså på ingen måde baseret på et dårligere grundlag end normalt.”
Læs også: 6 gode råd: Sådan undgår du influenza på jobbet
- Men normalt tager det op til 10 år at udvikle en vaccine. Hvordan kan udviklingen nu ske på mindre end et år?”Grunden til at det kan lade sig gøre er, at investeringerne har været fuldstændig gigantiske, idet man har løbet en kæmpe risiko ved at udvikle vaccinerne sideløbende med hinanden. Normalt udvikler man en vaccine ad gangen, så man ikke sætter en for stor investering i gang. Så ét vaccineforsøg har mulighed for at give viden til det næste, og det sikrer, at man investerer i det rigtige. Men det har der ikke været tid til her. I stedet har man sat 100 vaccineforsøg i gang samtidigt. Især fase 3-forsøgene, som 12 vacciner er i gang med, er vanvittigt dyre, fordi der er mange mennesker, der er med i forsøgene, og fordi personalet følger forsøgspersonerne så tæt.”
- Alligevel har der vel ikke været tid til at undersøge langtids-bivirkninger?
”I og med at forsøgene kun har fulgt deltagerne i højst 6-8 måneder har vi naturligvis ikke dokumentation, der udelukker, at der måtte komme andre bivirkninger efter et til to år. Og sådan er det med meget ny medicin, der kommer på markedet. Så det kommer an på en samlet vurdering af, hvad risikoen er. Og den vurdering kan jeg ikke give dig, før jeg har set resultaterne. Men én ting kan jeg i hvert fald love dig og alle FOAs medlemmer: At når jeg mener, at det er tilstrækkeligt belyst, efter at jeg har set materialet, så er jeg villig til at sætte min egen krop ind på det. Men det vil være useriøst af mig at sige, at jeg vil det, før jeg har set resultaterne.”
- Men kan det ske, at Lægemiddelstyrelsen godkender et præparat, der ikke er helt sikkert?
”Nej, det kan ikke ske. Hvis Lægemiddelstyrelsen godkender det, så vil de sikre, at den gavnlige effekt ved vaccinen overstiger de eventuelle bivirkninger, lige som hos ethvert andet lægemiddel. Sådan skal det være, og sådan er det altid. Vi giver ikke medicin eller vacciner til folk, hvis vi ved, at skadevirkningen er større end den gavnlige effekt. Og når der er tale om raske personer, skal der være en stor effekt og en meget begrænset bivirkning. Hvilket ikke er det samme, som at der ikke kommer bivirkninger.”
- Hvilken slags bivirkninger?
”Vi kan allerede nu sige, at der vil være bivirkninger, lige som vi også oplever ved andre vacciner. For eksempel træthed i dagene efter, hovedpine, nogle føler måske lidt ømhed eller rødme, der hvor de har fået vaccinen.”
- Så du mener ikke, at man kan tale om at være forsøgskanin, når vaccinen bliver rullet ud?
”Jeg vender mig meget imod det begreb. Der er ikke tale om at nogen skal være forsøgskanin. Hvis der er nogen, der har været med i et forsøg, så er der de 450.000 mennesker, der har meldt sig frivilligt til at være med i vaccineforsøgene i ren næstekærlighed. Der er 30-60.000 mennesker med i hvert eneste vaccineforsøg. De bliver fulgt tæt de næste tre år i hvert fald, så vi kan se, hvis vaccineeffekten for eksempel viser sig ikke at holde så godt i tiden efter, vaccinen er udført, som vi troede. Så ved vi det fire-fem måneder før, det viser sig hos resten af befolkningen. Processen slutter ikke i december. Det kommer til at vare, fire, fem og seks år endnu.”
Det sker nu ...
Den 29. december træffer Det Europæiske Lægemiddelagentur EMA afgørelse på vegne af 27 medlemslande om Pfizer/BioNtechs vaccine, og den 12. januar træffes afgørelse om Modernas.
Hvis EMA anbefaler vaccinerne, udsteder EU-kommissionen herefter en tilladelse til markedsføring i samtlige EU-lande – også i Danmark.
Medicin eller en vaccine mod coronavirus SARS-CoV-2 kan kun godkendes til brug bredt i befolkningen, hvis der foreligger solid og tilstrækkelig dokumentation om præparatets effekt og sikkerhed fra store, videnskabelige forsøg med tusindvis af mennesker fra såkaldte fase 3-forsøg.
Næste kandidat, der formentlig vil ansøge om godkendelse i EMA forventes at blive den svensk-britiske vaccine fra Astra Zeneca/Oxford University.
Kilde: Lægemiddelstyrelsen
